Цели:
Обучающие: Повторить строение атома и явление аллотропии на примере углерода; рассмотреть строение, сравнение свойств и применение алмаза и графита; дать понятие об аморфном углероде и адсорбции, их практическом применение;
Развивающие: Разбирать химические свойства углерода, закреплять дальнейшие навыки написания уравнений химических реакций на примере свойств углерода; продолжить формирование умения сотрудничества на уроке, работы в коллективе;
Воспитательные: Воспитывать любознательность, самостоятельность; развивать познавательный интерес учащихся к предмету, умение выделять главное, сравнивать.
Оборудование: мультимедийный проектор, экран, модели кристаллических решеток алмаза и графита, образцы изделий из графита (карандаши, электроды), сажи (чернила, резина), древесный уголь, чернила, фильтр, пробирки, активированный уголь.
Тип урока: урок получения новых знаний
Методы: словесные (рассказ, проблемное изложение), наглядные (флипчарт, видеофрагмент), эвристические (письменные и устные упражнения)
Технологии: элементы педагогики сотрудничества, личностно-ориентированное обучение (компетентностно-ориентированное обучение), информационно-коммуникативная технология, здоровьесберегающая образовательная технология.
Дидактические материалы к учебному занятию:
периодическая система, карточки для закрепления изученного материала «Характеристика углерода по его положению в ПСХЕ»;
карточки с изображением противогаза, делительной воронки, бытового фильтра, пылесоса, активированного угля;
карточки для проверки первичного усвоения материала урока «Вставь пропущенные слова»;
флипчарт «Углерод», видео фрагмент
План урока:
1. Орг.момент.
2. Объяснение нового материала.
3. Закрепление.
4. Итог урока.
Ход урока.
1. Орг.момент.
Открываю страницы №1, 2, 3.
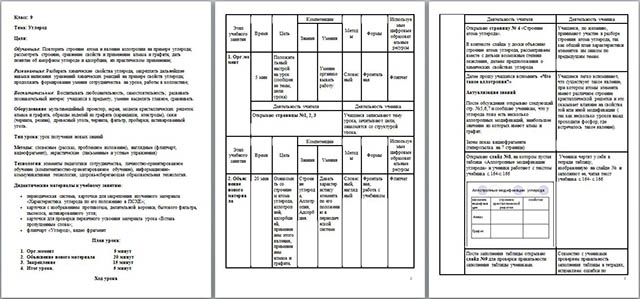
2. Объяснение нового материала.
Ознакомить со строением атома углерода, аллотропией, адсорбцией, применением этого явления, применением алмаза и графита.
Открываю страницу № 4 «Строение атома углерода».
В контексте слайда у доски объясняю строение атома углерода, рассматриваем вместе с детьми возможные степени окисления, делаем предположения о химических свойствах углерода.
Далее прошу учащихся вспомнить «Что такое аллотропия?»
Актуализация знаний.
После обсуждения открываю следующий стр. №5,6,7 и сообщаю ученикам, что у углерода тоже есть несколько аллотропных модификаций, наибольшее значение из которых имеют алмаз и графит.
Затем показ видеофрагмента (гиперссылка на 7 странице)
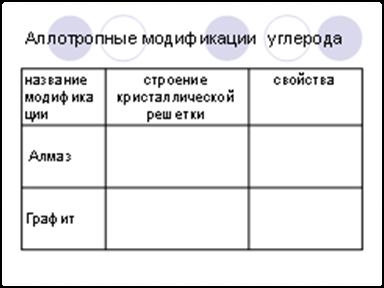
Открываю слайд №8, на котором пустая таблица «Аллотропные модификации углерода» и ученики работают с текстом учебника с.164-с.166
После заполнения таблицы открываю слайд №9 для проверки правильности заполнения таблицы учениками.
Весь материал - в документе.
 Получите свидетельство
Получите свидетельство Вход
Вход













 Конспект урока по химии "Углерод" (59.34 КB)
Конспект урока по химии "Углерод" (59.34 КB)
 0
0 821
821 111
111 Нравится
0
Нравится
0


