Тема урока «Водород, физические, химические свойства водорода. Изотопы водорода»
8 класс
Форма проведения веб-квест
2018 год
Цель: Познакомить учащихся с элементом водородом в свете ПСХЭ. Дать характеристику физическим и химическим свойствам водорода. Рассмотреть основные способы получения и применение водорода, изотопов водорода
Урок проводится в виде веб-квеста: пересказ (понимание темы на основе представления материалов из разных источников в новом формате) создание презентации, плаката, рассказа, решения задач
Необходимые ресурсы для выполнения задания: ПК, доступ и Интернет, учебник «Химия 8 класс», дополнительная литература.
Ход урока
Задание.
Побуждение к познанию
Начнем же список с водорода,
Поскольку первый элемент.
Он образует кстати, воду-
Весьма существенный момент.
В ходе выполнения работы необходимо изучить следующие вопросы: изучить физические и химические свойства водорода, методы получения водорода в промышленности и в лаборатории, значением водорода для организма человека и природы
Для решения данных вопросов необходимы специалисты:
Роль 1. Историк
Роль 2. Химик
Роль 3. Биолог
Роль 4. Эколог
Распределим обязанности между ними.
Порядок работы:
Выберите себе ту роль, которая вам ближе и с которой, как вам кажется, вы можете справиться.
Выбравшие себе одну и туже роль, можете объединиться в микрогруппу или работать индивидуально до тех пор, пока не наступит этап выработки общей точки зрения на проблему (7-10 мин).
После работы вы должны обсудить результаты работы в микрогруппе и подготовить совместный отчет (3 мин)
Для оформления результатов вы можете использовать:
- мультимедийные презентации;
- обобщающие таблицы;
- творческие отчеты
- кластеры.
- различные виды схем и диаграммы.
Критерии оценки
Работа в группе будет оцениваться.
В зависимости от набранных баллов будет выставлена оценка за весь квэсти оценки каждому «специалисту».
| Критерии оценки технического оформления | Глубина и оригинальность содержания | Качество оформления | Грамотность изложения | Успешность коллективной работы |
|
|
|
|
|
|
Ресурсы:
Вы должны использовать при выполнении заданий:
- ссылки на Интернет ресурсы;
- энциклопедии, справочники, информацию.
Роль 1. Химик.
Как химик, вы должны охарактеризовать следующие вопросы:
1. Физические свойства водорода
2.Химические свойства вод
3.Нахождение в природе
https://ru.wikipedia.org/wiki/Водород
https://ru.wikipedia.org/wiki/Водород
https://interneturok.ru › Химия › 8 класс
Информация 1
Первые упоминания о получении горючего газа при действии кислот на металлы встречаются в работах многих химиков (скорее даже не химиков, а алхимиков) в XVI-XVII веках. Первым стал рассматривать водород как химический элемент француз А.Л.Лавуазье, который в 1787г.установил, что при горении на воздухе этот газ образует воду. Поэтому он дал элементу и соответствующему ему газу название hydrogene ( по-греческиhydor- вода, а gennao-рождаю). В середине XIXвека в России утвердилось произношение символа элемента по-французки ( «аш»). Длительное время положение водорода в ПСХЭ было двойственным- его размещали и в 1-ой и в 7-ой группах, но по последним рекомендациям ИЮПАК водород- элемент 1 группы.
Водород плохо растворим в воде еще хуже в органических растворителях, а в некоторых металлах водород растворим очень хорошо. Так, в 1 объеме палладия растворяется 850 объемов водорода. Но палладий дорог, и как аккумулятор водорода для практических целей ( например, для двигателя работающего на экологически чистом водородном топливе) его использовать не выгодно.
Водород - самый легкий газ. Если шар объемом 22,4м3 наполнить водородом. То в воздухе он может поднять груз массой 29-2=27кг. В первой половине XXв. началось строительство летательных аппаратов большой грузоподъемности- дирижаблей, которые наполняли водородом. Но водород- взрывоопасный газ, и в 1930-е г.г. с дирижаблями произошло несколько крупных аварий. После этого строительство дирижаблей с водородом во всем мире на многие годы прекратилось.
Атом водорода (H)
| Положение в ПСХЭ | Состав атома | Строение атома | Свойства атома |
| 1-я группа главная подгруппа 1-й период | В ядре 1 протон вокруг ядра вращается 1 электрон | H+1)¹ | Не металл |
| | Ar(H)=1,008 | Электронная формула 1S¹ | Валентность=1 |
Молекулы водорода (H2)
| Состав молекулы | Строение молекулы | Свойства молекулы |
| (2 атома водорода) | H-H | Молекула неполярна |
| | Связь ковалентная, не полярная | Молярная масса= 2г/моль |
Задача проблемная
Наш космический корабль совершил вынужденную посадку на неизвестной планете. Приборы показали, что в образцах почвы обнаружены следующие металлы: медь, железо, цинк, магний, алюминий, серебро. Для взлета корабля необходим водород. В корабельных аккумуляторных батареях содержится серная кислота. Предложите способы получения водорода.
Химические свойства

Водород легче воздуха, поэтому соберем его в пробирку, перевернутую вверх дном, затем обязательно проверим водород на чистоту. Если водород чистый, то при его поджигании мы услышим глухой звук «пах». А если он смешан с воздухом- звук свистящий. А теперь изучим химические свойства водорода.
1.Взаимодействие с простым веществом О2
2H2+O2→2H2O
Опыт: Получив водород в аппарате Киппа, проверяем его на чистоту. Чистый водород горит бесцветным пламенем. Если поднести стеклянную пластинку, мы увидим, что она запотела, появились капельки воды.
2.Взаимодействие со сложными веществами
H2+CuO Cu+H2O
Cu+H2O
Опыт: Водород пропускают через горизонтально закрепленную в штативе стеклянную трубку, в котором находится оксид меди. Трубка нагревается с помощью спиртовки. Черный оксид превращается в красную медь.
После работы с источниками информации обсудить результаты работы в микрогруппе и подготовить совместный отчет. Для подготовки отчета можно использовать презентацию или кластер.
Роль 2. Историк
Как историк, рассмотрите историю открытия состава водорода, какие ученые работали над решением этой загадки
abouthist.net/xvii-vek/istoriya-otkrytiya-vodoroda.html
alhimikov.net/otkritie_elementov/H.html
https://interneturok.ru › Химия › 8 класс
Информация 1:
Еще в 16-17 веке такие выдающиеся экспериментаторы как Теофраст Парацельс, Роберт Бойль, Джозеф Пристли, Михайло Ломоносов получали горючий газ, действуя на металлы кислотами. Но они считали, что при этом образуется «флогистон». Знаете ли вы, что это такое? Это некая гипотетическая «сверхтонкая материя» — «огненная субстанция», якобы наполняющая все горючие вещества и высвобождающаяся из них при горении. Но эта теория была ошибочной.
Настоящим первооткрывателем водорода считают английского ученого Генри Кавендиша, который в 1766 году не только получил водород но и первым подробно описал его физические и химические свойства. В 1781 году английский ученый, наблюдая горение водорода на воздухе: 2Н2 + О2 = 2Н2О установил, что водород при горении превращается в чистую воду.
В 1783–1784 гг. А. Лавуазье совместно с Ж. Менье осуществили термическое разложение воды и установили, что она состоит из кислорода и водорода и назвали его гидрогениум, что означает «рождающий воду».
После работы с источниками информации обсудить результаты работы в микрогруппе и подготовить совместный отчет. Для подготовки отчета можно использовать презентацию или текстовый редактор.
Роль 3. Биолог.
как, специалисты в этой области, вы должны объяснить роль изотопов водорода для всех живых организмов. Рассмотреть и обсудить следующие вопросы:
Нахождение водорода в организме человека
Роль водорода в организме человека
https://ru.wikipedia.org/wiki/Водород
chem21.info/info/1674140/
5terka.com/node/10486
https://moydietolog.ru/vodorod
sinergichnost.ru/sekrety-zdorov-ya/vodorod-e-to-toplivo-zhizni
https://otvet.mail.ru/question/15499172
www.perekis.ru/znachenie_dlya_organizma.html
После работы с источниками информации обсудить результаты работы в микрогруппе и подготовить совместный отчет. При подготовке отчета можно использовать презентацию или текстовый редактор.
Роль 4.Эколог
1.Необходимо выделить экологические проблемы изотопов водорода
2. Применение водорода и изотопов водорода в промышленности
https://ru.wikipedia.org/wiki/Изотопы_водорода
polyguanidines.ru/a_hlorgeksidin&vodorod&5.htm
https://ru.wikipedia.org/wiki/Дейтерий
https://ru.wikipedia.org/wiki/Тритий
https://ru.wikipedia.org/wiki/Протий
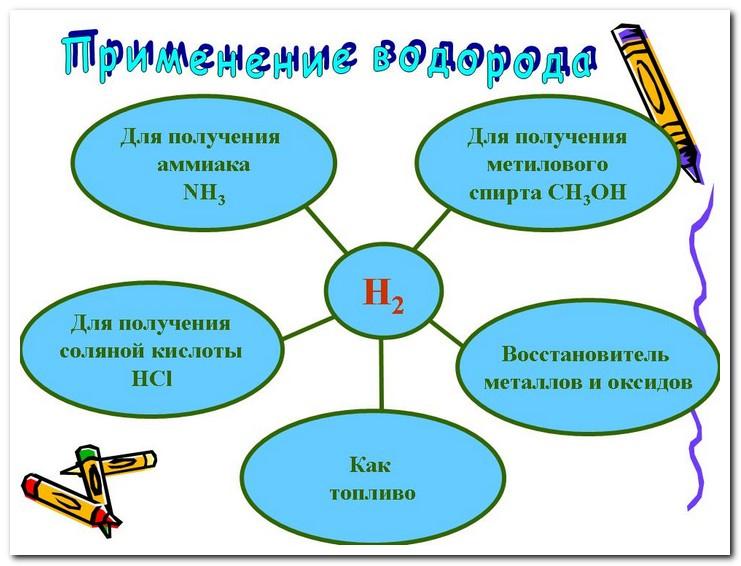
Отчет: Ваша работа должна быть представлена в виде презентации, кластера, схемы в которой вы отразите ваши ответы на главные вопросы темы
Результат работы: каждая группа выступает с публичной защитой (3мин)
Для закрепления материала небольшое задание (индивидуальная работа) ( 2-3 мин)
Вариант 1
1.Водород в лаборатории получают по реакции (закончить уравнение):
Zn + HCl→__________________
2.Полученный газ можно собрать методом вытеснения воды, используя прибор:
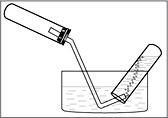


А) Б) В)
3. Водород можно собрать методом вытеснения воды, так как он:
А) плохо растворим в воде Б) легче воздуха В) хорошо растворим в воде
Г) тяжелее воздуха.
4. Водород открыл: А) Д.И. Менделеев Б) Карл Шееле В) Генри Кавендиш
Г) Антуан Лавуазье
5. Для получения водорода в лаборатории используют
А) Газометр Б) Аппарат Киппа В) Сосуд Дьюара Г) Плоскодонную колбу
Вариант II
1.Водород в лаборатории получают при взаимодействии железных стружек с раствором соляной кислоты по реакции: ________________________________
2.Полученный газ можно собрать методом вытеснения воздуха, используя прибор:



А) Б) В)
3.Водород можно собрать методом вытеснения воздуха, так как он:
А) плохо растворим в воде Б) легче воздуха В) хорошо растворим в воде
Г) тяжелее воздуха.
4. Чтобы проверить наличие водорода в пробирке нужно:
А) Тлеющую лучинку внести внутрь пробирки
Б) Перевернуть пробирку и налить в нее воду
В) Не переворачивая пробирку, поднести ее к пламени спиртовки
5. Водород легче воздуха: А) в 2 раза Б) в 10 раз В) в 14,5 раз Г) в 29 раз.
Проверка выполнения теста( 2 мин)
Домашнее задание: повторить материал, найти информацию о значении перекиси водорода
Рефлексия
8
 Получите свидетельство
Получите свидетельство Вход
Вход












 Водород: свойства, применение (148.64 KB)
Водород: свойства, применение (148.64 KB)
 0
0 367
367 2
2 Нравится
0
Нравится
0


