
Свободные атомы
Простые вещества
Сложные вещества

©Автор: Ваганов Андрей Игоревич,
учитель химии и физики
МОУ СОШ №2 г.Ростова.

Известно 95 элементов
Большой атомный радиус
Отдают внешние электроны (1 – 3)
Характерны ионная и металлическая химические связи

Известно 23 элемента
Небольшой атомный радиус
Принимают внешние электроны (1 – 4)
Характерны ионная и ковалентная химические связи

(95) (23)
˃
R ат R ат
Отдают внешние e̅ Принимают внешние e̅
1 – 3 e̅ 1 – 4 e̅
Me O – n e̅ ↔ Me n+
не Me O + n e̅ ↔ не Me n -
Характерны ионная
и металлическая
химические связи
Характерны ионная
и ковалентная
химические связи


Твердые
(все Ме, кроме Hg)
Жидкая
( Hg – ртуть )
 1000°С ) W – вольфрам Легкоплавкие ( t пл Hg – ртуть " width="640"
1000°С ) W – вольфрам Легкоплавкие ( t пл Hg – ртуть " width="640"
Тугоплавкие
( t пл 1000°С )
W – вольфрам
Легкоплавкие
( t пл
Hg – ртуть

Твердые
( Cr – хром )
Мягкие
(Щелочные металлы )
 5 г/см 3 ) Pb, Hg, Cd Легкие ( ρ Al, Li, Mg " width="640"
5 г/см 3 ) Pb, Hg, Cd Легкие ( ρ Al, Li, Mg " width="640"
Тяжелые
( ρ 5 г/см 3 )
Pb, Hg, Cd
Легкие
( ρ
Al, Li, Mg

Худшая
( Hg, Pb, W)
Лучшая
( Ag, Al, Au, Ag, Fe)
Электропроводность металлов объясняется наличием
в их структуре общих свободных электронов

Объясняется наличием свободных электронов, которые в результате своего движения обеспечивают быстрое выравнивание температуры металла.

Объясняется смещением слоев атомов без разрыва химических связей.

Обеспечивается отражающей способностью
свободных электронов.


Твердые
( C, P, S)
Жидкий
( Br 2 – ртуть )
Газы
( O 2 , H 2 , N 2 , Cl 2 , F 2 , O 3 )



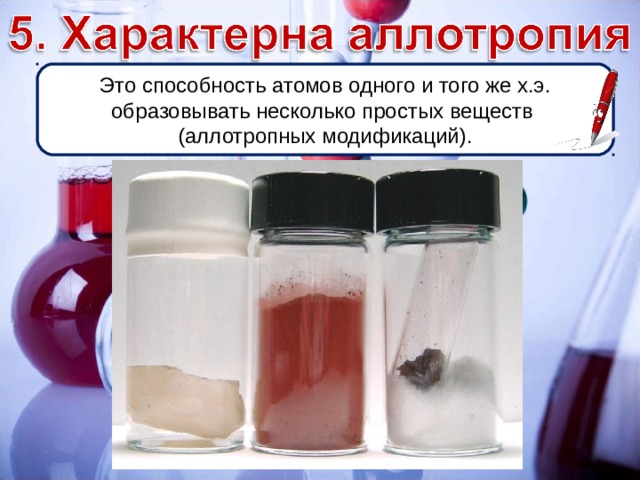
Это способность атомов одного и того же х.э. образовывать несколько простых веществ
(аллотропных модификаций).

а) разное число атомов в молекуле
О 2 (кислород)
О 3 (озон)
Р (фосфор красный)
Р 4 (фосфор белый)

б) образование разных кристаллических форм
( С - углерод )
Алмаз
Графит
Уголь

Характерен только для графита (С),
йода ( I 2 ) , кремния (Si) .

§14-15, с.85 №4 (у),
с.92 №1,2 (у), №3-5 (п).
 Получите свидетельство
Получите свидетельство Вход
Вход












 Простые вещества металлы и неметаллы (8.27 MB)
Простые вещества металлы и неметаллы (8.27 MB)
 0
0 267
267 32
32 Нравится
0
Нравится
0


