
ЩЕЛОЧНОЗЕМЕЛЬНЫЕ МЕТАЛЛЫ Be и Mg

Расположение щелочноземельные металлы в ПСХЭ
- II группа главная подгруппа;
- Во всех соединениях проявляют степень окисления +2.

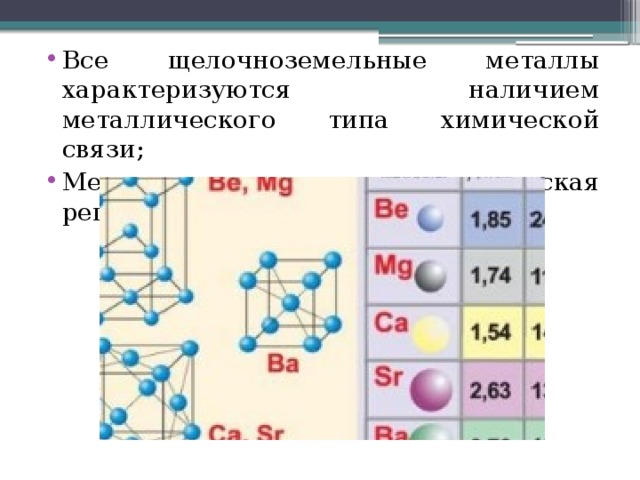
- Все щелочноземельные металлы характеризуются наличием металлического типа химической связи;
- Металлическая кристаллическая решетка.



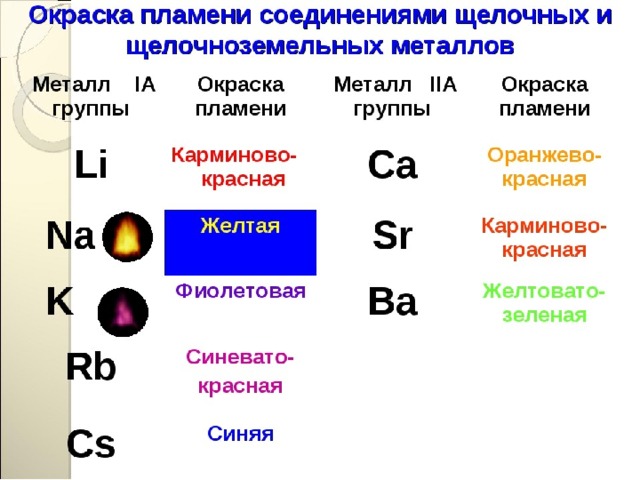

Получение
разложение нитратов или карбонатов
CaCO 3 t°= CaO + CO 2
2Mg(NO 3 ) 2 t°= 2MgO + 4NO 2 + O 2




Домашнее задание
- Ca→CaO→Ca(OH) 2 →Ca(NO 3 ) 2 ;
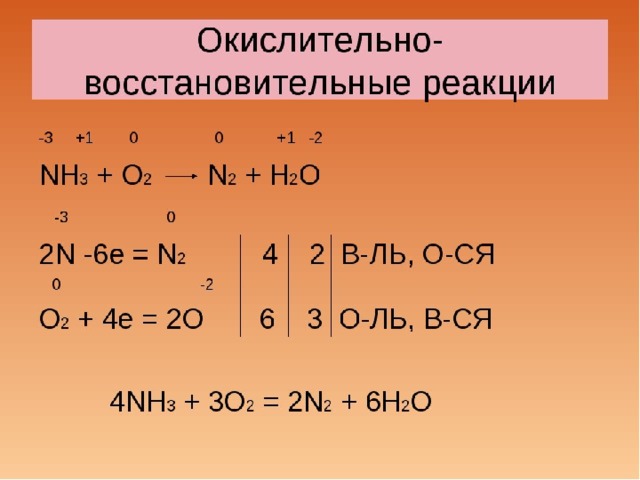
- Расставьте коэффициенты в реакции используя метод электронного баланса:
СuS + HNO 3 (разбавленная) = Cu(NO 3 ) 2 + S + NO + H 2 O
 Получите свидетельство
Получите свидетельство Вход
Вход













 Презентация к уроку по теме "Щелочноземельные металлы" (1.62 MB)
Презентация к уроку по теме "Щелочноземельные металлы" (1.62 MB)
 0
0 1861
1861 347
347 Нравится
0
Нравится
0


