Спецификация
контрольных измерительных материалов для проведения
диагностики знаний учащихся
по ХИМИИ по теме «Металлы»
9 класс
1. Назначение КИМ – оценить уровень общеобразовательной подготовки по химии по теме «Металлы», 9 класс.
2. Документы, определяющие содержание КИМ
Содержание экзаменационной работы определяет Федеральный компонент государственного стандарта основного общего образования по химии (приказ Минобразования России от 05.03.2004 № 1089 «Об утверждении Федерального компонента государственных стандартов начального общего, основного общего и среднего (полного) общего образования»).
3. Характеристика структуры и содержания КИМ
Каждый вариант экзаменационной работы содержит 12 заданий. В числе этих заданий:
задания с порядковыми номерами 1,2,4,6-8 - базового уровня сложности, ответ на которые записывается в виде одной цифры;
задания с порядковыми номерами 3,5,9 – повышенного уровня сложности, на установление соответствия между элементами двух множеств, ответ на которые записывается в виде последовательности трёх или четырёх цифр;
задания с порядковыми номерами 10, 11, 12 высокого уровня сложности, которые предполагают запись развёрнутого ответа.
4. Продолжительность итоговой диагностической работы.
На выполнение итоговой диагностической работы отводится 45 минут.
5. Дополнительные материалы и оборудование.
В процессе выполнения итоговой диагностической работы по химии разрешается использовать следующие материалы и оборудование:
– Периодическая система химических элементов Д.И. Менделеева;
– таблица растворимости солей, кислот и оснований в воде;
– электрохимический ряд напряжений металлов;
– непрограммируемый калькулятор.
6. Система оценивания выполнения отдельных заданий и итоговой диагностической работы в целом
Верное выполнение каждого из заданий 1,2,4,6-8 оценивается 1 баллом.
Верное выполнение каждого из заданий 3,5,9 максимально оценивается 2 баллами. Если в ответе на эти задания допущены ошибки, то задание считается выполненным частично и оценивается с шагом 0,5 балла.
Задания 10, 11, 12 с развернутым ответом могут быть выполнены обучающимися разными способами. Поэтому приведенные в критериях оценивания образцы ответов следует рассматривать лишь как один из возможных вариантов ответа. Каждый верно выполненный элемент ответа оценивается 1 баллом, причём максимальный балл за каждое из заданий с порядковыми номерами 10 и 11 составляет 3 балла, задания 12 – 4 балла.
Таблица перевода баллов в отметки по пятибалльной шкале
| Отметка по пятибалльной шкале | «2» | «3» | «4» | «5» |
| Первичные баллы | 1 – 11 | 12 – 16 | 17 – 21 | 22 – 24 |
Обобщенный план варианта контрольных измерительных материалов
для проведения итоговой диагностической работы
по ХИМИИ
9 класс
Уровни сложности заданий: Б – базовый; П – повышенный; В – высокий.
| № | Проверяемые элементы содержания | Коды проверяемых элементов содержания | Коды проверяемых требований к уровню подготовки выпускников | Уровень сложности задания | Максимальный балл за выполнение задания |
| 1 | Строение атома. Строение электронных оболочек первых 20 элементов Периодической системы Д.И. Менделеева | 1.1 | 2.5.1 | Б | 1 |
| 2 | Периодический закон и Периодическая система химических элементов Д.И. Менделеева | 1.2 | 1.3 2.2.2 | Б | 1 |
| 3 | Физические свойства металлов
|
|
| П | 2,5 |
| 4 | Получение металлов |
|
| Б | 1 |
| 5 | Сплавы
|
|
| П | 2,5 |
| 6 | Химические свойства простых веществ - металлов | 3.1.1 | 2.2.2 2.3.2 | Б | 1 |
| 7 | Химические свойства основных и амфотерных оксидов | 3.2.1 | 2.3.3 | Б | 1 |
| 8 | Химические свойства оснований. | 3.2.2 | 2.3.3 3.2.3 | Б | 1 |
| 9 | Химические свойства простых веществ. Химические свойства сложных веществ | 3.1 3.2 | 2.3.2 2.3.3 | П | 3 |
| 10 | Степень окисления химических элементов. Окислитель и восстановитель. ОВР | 2.6 | 2.4.2 2.5.3 | В | 3 |
| 11 | Вычисление массовой доли растворенного вещества в растворе. Вычисление количества вещества, массы или объема вещества по количеству вещества, массе или объему одного из реагентов или продуктов реакции | 4.5.2 4.5.3 | 2.8.2 2.8.3 | В | 3 |
| 12 | Химические свойства простых веществ. Химические свойства сложных веществ. Взаимосвязь различных классов неорганических веществ. Реакции ионного обмена и условия их осуществления | 3.1 3.2 3.3 4.4 | 2.4.6 2.5.3 | В | 4 |
Контрольная работа «Металлы» 9 класс
Вариант-1
1. На приведенном рисунке изображена модель атома
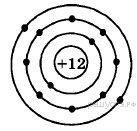
1) магния
2) кальция
3) лития
4) калия
2. Наиболее сильными основными свойствами обладает оксид
1) магния
2) бериллия
3) алюминия
4) натрия
3. Установите соответствие между металлом и его характерным свойством.
МЕТАЛЛ СВОЙСТВО
А) Ag 1) лучшая отражательная способность
Б) Cr 2) наиболее тугоплавкий
В) Au 3) самый тяжёлый
Г) W 4) самый пластичный
Д) Os 5) наиболее твёрдый
| А | Б | В | Г | Д |
|
|
|
|
|
|
4. В промышленности электролизом получают
алюминий
цинк
железо
свинец
5. Установите соответствие между легирующим элементом в сплаве и названием сплава.
СОСТАВ НАЗВАНИЕ СПЛАВА
А) Cu 50% Zn 1) дюралюминий
Б) Cu 20% Sn 2) мельхиор
В) Cu 20% Ni 3) латунь
Г) Al, Cu, Mn 4) бронза
5) сталь
| А | Б | В | Г | Д |
|
|
|
|
|
|
6. Железо реагирует с
1) хлоридом кальция
2) бромом
3) оксидом натрия
4) гидроксидом натрия
7. Оксид железа(III) реагирует с
1) гидроксидом меди(II)
2) хлоридом магния
3) серной кислотой
4) оксидом алюминия
8. В реакцию с раствором гидроксида калия вступает
1) ![]()
2) ![]()
3) ![]()
4) ![]()
9. Установите соответствие между названием вещества и реагентами, с которыми это вещество может взаимодействовать.
| НАЗВАНИЕ ВЕЩЕСТВА | РЕАГЕНТЫ | |||
| A) магний | 1) | |||
| Б) оксид натрия | 2) | |||
| B) гидроксид бария | 3) | |||
|
| 4) | |||
|
|
| |||
| А | Б | В |
| |
|
|
|
|
| |
10. Используя метод электронного баланса, расставьте коэффициенты в уравнении реакции, схема которой:
![]()
Определите окислитель и восстановитель.
11. В 73 г соляной кислоты с массовой долей ![]() 5% поместили избыток цинка. Вычислите объём выделившегося газа (н. у.).
5% поместили избыток цинка. Вычислите объём выделившегося газа (н. у.).
12. Дана схема превращений:
![]()
Напишите молекулярные уравнения реакций, с помощью которых можно осуществить указанные превращения. Для второго превращения составьте сокращённое ионное уравнение реакции.
 Получите свидетельство
Получите свидетельство Вход
Вход












 Контрольная работа по химии "Металлы. 9 класс" (115.5 KB)
Контрольная работа по химии "Металлы. 9 класс" (115.5 KB)
 0
0 1829
1829 4
4 Нравится
0
Нравится
0


