Цели урока:
образовательные: на примере алюминия закрепить знания учащихся об общих свойствах металлов; сформировать у учащихся понятие амфотерности на примере свойств гидроксида алюминия; закрепить и развить знания о классификации и свойствах гидроксидов в свете теории электролитической диссоциации,
развивающие: продолжить формирование умения давать характеристику элемента по его положению в Периодической системе; закрепить умения учащихся работать с лабораторным оборудованием,
воспитательные: развитие логического мышления, умений делать выводы на основе практического опыта.
Тип урока: комбинированный.
Педагогические технологии (СОТ)
- ИКТ (использование компьютерной презентации)
- системно-деятельстный подход
- проблемное обучение
- разноуровневое обучение
Методы обучения: объяснительно-иллюстративный, информационно-сообщающий, проблемный.
Формы работы: фронтальная, групповая, индивидуальная.
Оборудование и реактивы:
На столе учителя – гранулы и порошок алюминия, порошок серы, бенгальские свечи, растворы соляной кислоты - НСl и серной кислоты - Н2SО4; концентрированная азотная кислота - НNО3, пробирки; коллекция минералов, содержащих алюминий, горелка, пробиркодержатель.
На столах учащихся – растворы хлорида алюминия – А1С13, гидроксида натрия –NаОН, серной кислоты – Н2SО4, 2 пробирки.
Этапы урока:
1. Организационный момент – 2 мин.
2. Изучение новой темы:
а) актуализация знаний – 6 мин. ;
б) компьютерная презентация - 5 мин. ;
в) объяснение учителя – 12 мин. ;
г) лабораторная работа -5 мин. ;
д) компьютерная презентация - 3 мин.
3. Закрепление изученного материала - 10 мин.
4. Домашнее задание - 2 мин.
Ход урока
1. Организация класса – приветствие, проверка готовности учащихся к уроку.
Объявление учителем целей и задач урока, инструктаж о соблюдении правил безопасности при выполнении лабораторных опытов.
2. Изучение новой темы:
а) Актуализация знаний учащихся
Цель: на примере алюминия закрепить знания учащихся о свойствах металлов, умение характеризовать элемент по его положению в Периодической системе.
Учитель:
На сегодняшнем уроке мы с вами продолжаем изучение металлов и подробнее познакомимся с одним из самых распространенных и значимых в нашей жизни металлом – алюминием. И, как всегда, при изучении простого вещества начнем с характеристики химического элемента.
Далее - фронтальная беседа по вопросам. Учащиеся записывают характеристику элемента в тетрадях
1. Место А1 в Периодической системе.
- Алюминий - элемент с порядковым № 13, находится в 3-ем периоде, 3-ей группе, главной подгруппе, атомная масса элемента – 27.
2. Состав ядра атома А1.
- В ядре атома алюминия 13 протонов и 14 нейтронов.
3. Электронная формула А1. (один из учащихся записывает формулу на доске)
А1))) 1s22s22р63s23р1
2е 8е 3е
5. Число валентных электронов, свойства элемента.
- На последнем электронном уровне у алюминия 3 электрона, до завершения электронного уровня не хватает 5, поэтому элемент будет проявлять восстановительные свойства, отдавая 3 электрона, степень окисления его будет + 3.
6. Как проявляются восстановительные свойства алюминия по сравнению с соседними элементами в периоде и группе?
- Восстановительные свойства в группе у алюминия будут выражены сильнее, чем у бора, но слабее, чем у галлия, т. к. сверху вниз в группе увеличивается число электронных уровней, валентные электроны отдаляются от ядра и легче отщепляются. В периоде у алюминия восстановительные свойства выражены сильнее, чем у кремния, но слабее, чем у магния. Слева направо размеры атомов уменьшаются, поэтому их способность отдавать электроны снижается.
6. В периоде алюминий стоит между типичным металлом - магнием и неметаллом - кремнием. Какими свойствами, по- вашему, будет он обладать?
- Свойствами переходного элемента.
7. А что вы можете сказать из собственного опыта о свойствах простого вещества – алюминия?
- Ответы учащихся.
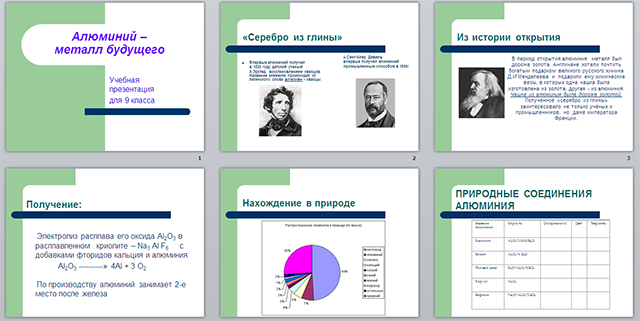
б) Нахождение алюминия в природе и его получение
(компьютерная презентация, подготовленная группой учащихся)
Просмотр слайдов презентации:
1. Содержание алюминия в земной коре (диаграмма, показывающая, что алюминий занимает 3-е место по содержанию в земной коре после кислорода и кремния).
2. Нахождение алюминия в природе.
Полную информацию смотрите в файле.
 Получите свидетельство
Получите свидетельство Вход
Вход












 Конспект и презентация урока по химии по теме «Алюминий» (0.13 MB)
Конспект и презентация урока по химии по теме «Алюминий» (0.13 MB)
 0
0 826
826 173
173 Нравится
0
Нравится
0


